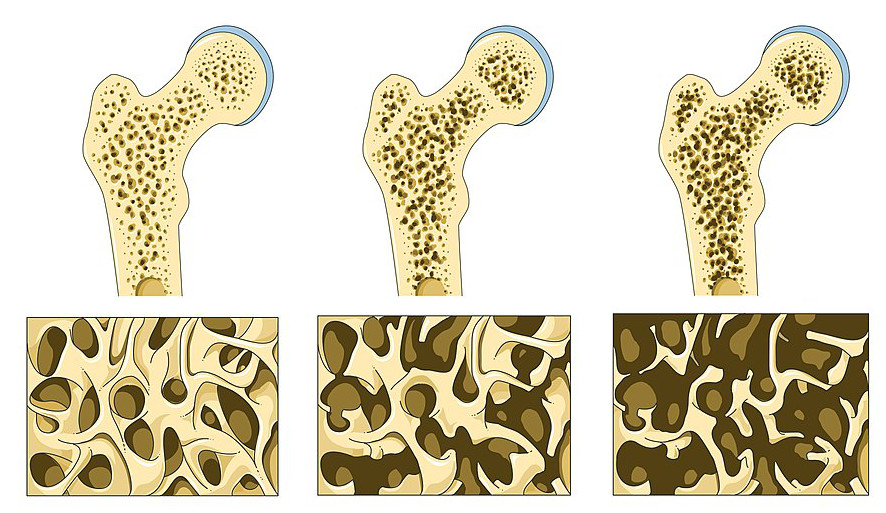
„Osteoporose ist eine systemische Skelettkrankheit. Sie ist gekennzeichnet durch eine niedrige Knochenmasse aufgrund eines übermäßigen, vorangegangenen Knochenmaße-verlustes und einer dadurch bedingten zunehmenden Zerstörung der Knochenstruktur mit der Folge einer krankhaft erhöhten Knochenbrüchigkeit.“
Dies ist die klassische und gut verständliche Definition der Osteoporose. Diese Definition hat einen entscheidenden Nachteil. Sie beantwortet nicht die entscheidende Frage, welche die Osteoporosediskussion bis heute beherrscht: Wie stelle ich fest, dass eine „krankhaft erhöhte Knochenbrüchigkeit“ besteht.
Dazu aber später. Zunächst soll mit ein paar Schlagzeilen die Bedeutung des Themas für Ihre individuelle Gesundheit dargestellt werden.
Jede 3. Frau und jeder 4. Mann bekommen im Laufe ihres Lebens Osteoporose.
6% der über 50-jährigen Männer und 24% der über 50-jährigen Frauen haben Osteoporose.
Je nach Lokalisation ist mit einer osteoporosebedingten Fraktur ein gegenüber der Altersgruppe mehrfach erhöhtes Sterberisiko verbunden, welches sich aus den Komplikationen durch die zwangsweise Ruhigstellung und verminderte körperliche Aktivität erklärt (Lungenembolie nach Schenkelhalsbruch, …).
Im Praxisalltag spielen natürlich nicht die tödlichen Komplikationen, sondern die chronischen Schmerzen aufgrund der Osteoporose eine Rolle.
Zum besseren Verständnis darf ich zwei bildliche Vergleiche aus der Technik bemühen, obwohl natürlich ein Vergleich zwischen biologischen Vorgängen einerseits und technischen Abläufen andererseits nur eingeschränkt möglich ist.
Durch die vermehrte Knochenbrüchigkeit kommt es bei Belastungsspitzen zunehmend zu mikroskopisch kleinen Einbrüchen des Knochens unmittelbar unter dem Gelenkknorpel bzw. der Bandscheibe. Der Vorgang ist in etwa vergleichbar dem allmählichen Absinken eines Daches, bei dem im Dachstuhl einzelne Stützen nachgeben. Das Dach – bzw. in unserem Fall die Gelenkfläche bzw. die Grund- oder Deckplatte des Wirbelkörpers – wird unregelmässiger und weniger belastbar.
Ein anderes, häufig für die Veranschaulichung verwendetes Bild sind die zunehmenden Risse in einer asphaltierten Straße deren Unterbau durch Witterungseinflüsse immer weniger tragfähig geworden ist. Auch hier wird zunächst die Tragschicht und dann die Oberfläche unregelmäßiger.
Je unregelmäßiger die Gelenkfläche, desto höher ist der Abrieb an der Gelenkfläche. Dieser Abrieb muß abtransportiert werden. Der Anfall von Abriebpartikeln führt zur Überlastung der Entsorgungswege. Die nicht abtransportierten Abriebpartikel führen letztlich zu einer Entzündung der Gelenkkapsel. Diese Entzündung verursacht den arthrosetypischen Schmerz und führt zu einer Vernarbung bzw. Schrumpfung des Gelenkkapsel. Bei geschrumpfter Gelenkkapsel ist das Gelenk weniger beweglich. Bei eingeschränkter Beweglichkeit verteilt sich die Beanspruchung auf eine geringere Gelenkfläche. Es setzt sich eine Negativspirale in Bewegung. Das Gelenk wird geschont – die zugehörige Muskulatur bildet sich zurück -, das Gelenk wird bei fehlender muskulärer Stabilisierung ungünstiger belastet, ….. .
Vermutlich haben Sie beim Lesen die Formulierung „schonungsbedingter Knochenabbau“ ohne Weiteres akzeptiert. Es ist eine Binsenweisheit: Jedes Organsystem, das nicht gefordert wird, baut ab. Das gilt für die Gefäße, das Herz, die Lunge und natürlich auch für den Knochen.
Daraus ergibt sich ein wichtiger Hinweis für die Behandlung:
An erster Stelle steht eine geeignete Trainingstherapie. Dazu zwei Beispiele aus der Sportmedizin: Bei Marathonläuferinnen traten in den 1990er Jahren (vor entsprechender Trainingsumgestaltung) häufiger als in der Normalbevölkerung osteoporosebedingte Ermüdungsbrüche des Schienbeinkopfes auf. Dreispringer (die pro Woche in der Regel nur 30 – 50 Dreisprünge absolvieren um den Knorpel nicht zu überlasten) haben im Schienbeinbereich eine 3-fach erhöhte Knochendichte im Vergleich zu Sportstudenten.
Das Thema Knochendichte möchte ich – nochmal – weiter nach hinten verschieben. Aber Sie merken schon, dass es offenbar als Kriterium für die Knochenbrüchigkeit verwendet wird.
Der adäquate Trainingsreiz für den Knochen ist also nicht das gleichmäßige Ausdauertraining, sondern die kurzfristige Spitzenbelastung. Eine hohe Geschwindigkeit der Drucksteigerung in der Knochenzelle signalisiert über die in der Zelle vorhandenen Dehnungsrezeptoren dem Ökosystem Zelle: Achtung, das war knapp vor der Bruchgrenze, wir müssen etwas tun, sprich Knochenmasse produzieren. Die Dauer der Drucksteigerung ist nicht entscheidend. Entscheidend ist der – wenn auch nur kurze – aber massive Druckanstieg in der Zelle.
Konkret lautet die Empfehlung neben dem nach wie vor aus anderen Gründen wichtigen Training von Ausdauer und Geschicklichkeit einmal wöchentlich ein kurzes Maximalkrafttraing zu absolvieren. Konsequentes Pilatestraining geht hier schon in die richtige Richtung. Ideal wären Betätigung von Beinpresse und Rückenstreckermaschine im Fitnessstudio (1 x 3 Wiederholungen mit dem Widerstand, der gerade eben 3 x überwunden werden kann). Alternativ zu den Übungen im Fitnessstudio können entsprechende isometrische Anspannungsübungen zu Hause durchgeführt werden.
Diese Trainingstherapie steht – konsequent über Jahre durchgeführt – in ihrer Effektivität über allen ärztlichen Maßnahmen. Möglicherweise wird dies in der öffentlichen Diskussion zuwenig betont, weil weder Ärzte noch Industrie davon profitieren.
Bei einer bereits bestehenden Osteoporose sind zusätzliche medikamentöse Maßnahmen notwendig und sinnvoll:
Die ausreichende Versorgung mit Vitamin D und Calcium ist eine wichtige Grundlage, bedarf aber keiner großen Diskussion, weil hier bei entsprechender Überwachung kein wesentliches Therapierisiko besteht.
Östrogene wirken dem Knochenabbau entgegen. Die Hysterie hinsichtlich Hormonsubstitution in der Menopause und damit verbundenes etwaiges Brustkrebsrisiko scheint sich gelegt zu haben. Die Indikation zu einer Hormontherapie sollte aber vom Frauenarzt gestellt werden.
Die sepzifische medikamentöse Therapie wird im Regelfall über einen von zwei alternativen Therapieansätzen durchgeführt. Nur in Sonderfällen oder bei Versagen der Erstlinienmedikamente wird zu exotischeren Methoden (Parathormonanaloga, Raloxifen) gegriffen.
Am meisten verbreitet ist die Therapie mit Biphosphonaten.
Biphosphonate können als Tabletten oder als Infusion verabreicht werden.
Die Substanzen werden in die Knochenmasse eingelagert und verbleiben über Jahre im Körper (Halbwertszeit bis zu 10 Jahren). Sie wirken hauptsächlich auf die knochenabbauenden Zellen (für zellbiologisch Interessierte: Hemmung der Protonen-ATP-ase, vorzeitige Apoptose, Verhinderung der Differenzierung der Osteoklastenvorläuferzellen zu Osteoklasten). Dadurch verschiebt sich das Gleichgewicht zwischen knochenabbauenden und knochenaufbauenden Zellen zugunsten der knochenaufbauenden Zellen.
Die Resorption über den Darm ist sehr unsicher (1-10 %). Bei 10 % der Patienten kommt es zu Magenbeschwerden. Selten kommt es zu Knochennekrosen im Kiefer oder zu atypsichen Oberschenkelbrüchen.
An zweiter Stelle stehen die RANKL- Antagonisten:
Die am meisten verbreitete Substanz (Denosumab) wird alle 6 Monate unter die Haut gespritzt, ähnlich wie die Heparinspritzen zur Blutverdünnung nach Operationen.
Vereinfacht gesagt handelt es sich um einen Antikörper gegen einen Botenstoff (Receptor Activator of NF Kappa Beta Ligand), der die Weiterentwicklung von Vorläufern der knochenabbauenden Zellen veranlasst. Der Antikörper blockiert diesen Signalweg. Die Entwicklung von knochenabbauenden Zellen wird also gehemmt.
Als Nebenwirkung ist eine erhöhte Infektanfälligkeit beschrieben. In der Laienpresse stark betont wird der Reboundeffekt, also ein – zeitlich befristet – überschiessender Knochenabbau nach dem Absetzen des Medikamentens.
Die diskutierte erhöhte Rate von bösartigen Erkrankungen ist nicht gut belegt.
Die Abwägung zwischen den beiden Therapieoptionen ist manchmal etwas schwierig. Beide Wege stellen aber eindeutig ein deutlich geringeres Risko dar als die unbehandelte Erkrankung.
Die Behandlungsdauer bemißt sich bei beiden Methoden in Jahren! Die erste Kontrolle des Therapieerfolges erfolgt nach drei Jahren.
Bleibt nur noch die Frage nach der Diagnose. Ich habe diese Thema etwas verschämt an den Schluß gerückt, weil wir zum einen immer noch keine gute Methode haben die Osteoporose frühzeitig zu erfassen und zum anderen bei bereits im MRT oder im Röntgen eindeutig zu diagnostizierender Osteoporose bereits wertvolle Zeit für die Therapie verloren gegangen ist.
Wir können die Festigkeit des Knochens nicht messen. Deshalb behelfen wir uns mit einem Ersatz: Wir messen die Knochendichte und unterschlagen dabei, dass die Festigkeit einer Konstruktion nicht nur von der Masse, sondern von der mehr oder weniger intelligenten Verteilung der Masse im Raum abhängt. Zur Veranschaulichung sei die gesteigerte Steifheit moderner Autokarosserien im Vergleich zu Konstruktionen aus den 50-er Jahren bei gleichzeitig geringerem Materialeinsatz angeführt.
Auch hier gibt es im Wesentlichen zwei Methoden:
Bei der DEXA wird die Abschwächung eines Röntgenstrahles, der an bestimmen Regionen (Hüfte, Lendenwirbelsäule) durch den Körper des Patienten geschickt wird gemessen.
Je stärker die Abschwächung, desto mehr röntgendichtes Gewebe (also vor allem Knochen oder Gefäßverkalkungen) liegt zwischen Strahlungsquelle und Meßstelle. Ein Differenzierung zwischen Knochenrinde und Knochenmark findet nicht statt.
Beim Q-CT wird – auch mit Röntgenstrahlen- ein Schnittbild der Lendenwirbelsäule erstellt, und die Knochendichte in einem bestimmten, definierten Gebiet innerhalb des Knochenmarkes gemessen. Durch Abnutzungserscheinungen veränderte Knochenanhangsgebilde oder Verkalkungen ausserhalb des Knochens können so ausgeklammert werden. Die Strahlenbelastung beträgt weniger als ein Zehntel gegenüber einem „ normalen“ CT, für das bei anderer Fragstellung sehr viel mehr Schnitte durchgeführt werden müssen.
Ich persönlich bevorzuge ganz eindeutig das Q-CT.
Früher vereinzelt in Praxen angewandte Ultraschallmethoden sind auf dem Rückzug und wurden zu keinem Zeitpunkt an einem großen Zentrum der Osteoporoseforschung (Bologna, Zürich, Wien, Münster) in der Routinediagnostik eingesetzt.
Die Aussagekraft der Knochendichtemessung kann bei grenzwertigen Befunden verbessert werden durch eine standardisierte Auswertung des Risikoprofiles (FRAX- Score der Uni Sheffield). Seit 2023 gibt es eine modifizierte Version des Scores, die vom Berufsverband der deutschen Orthopäden veröffentlicht wurde. In diesem Score werden Risikofaktoren wie Alter, Geschlecht, bisher stattgehabte Frakturen, bestimmte Medikamente sowie bestimmte Stoffwechselerkrankungen miterfasst.
Auch wenn die Knochendichtemessung nur eine Krücke ist, mit der wir uns in der Diagnostik behelfen, ist klar belegt, dass ab einem bestimmten Schwellenwert das Risiko für den Patienten so hoch ist, dass er eindeutig von der Behandlung profitiert.
Abschliessend vielleicht noch ein Wort zu den Messwerten.
Angegeben wird bei der Knochendichtemessung eine sogenannte Standardabweichung, der T-score. Standardabweichung bedeutet, dass, unter der Annahme einer Normalverteilung, die gemesssene Knochendichte sich in einer gewissen Entfernung vom Mittelwert der Bevölkerung bzw der Altersgruppe befindet.
Statistisch nicht ganz korrekt, darf ich folgendes Beispiel heranziehen: Die durchschnittliche Körpergröße eines Mannes in Niederbayern beträgt 175 cm. 68% der Männer in Niederbayern sind zwischen 165 und 185 cm groß. Ihre Größe weicht bis zu einer Standardabweichung vom Mittelwert ab. 95 % der Männer in Niederbayern sind zwischen 155 und 195 cm groß, ihre Größe weicht bis zu zwei Standardabweichungen vom Mittelwert ab. 99% aller Männner ….. .
Bei dem oben besprochenen und standardmässig eingesetzen Score wird die Wahrscheinlichkeit angegeben, mit der in den nächsten 3 Jahren eine osteoporosebedingte Fraktur am Unterarm, am Schenkelhals oder an der Wirbelsäule zu erwarten ist.
Bei einem Risiko von bis zu 3% sollte eine medikamentöse Behandlung durchgeführt werden.
Bei einem Risiko von über 3% soll eine medikamentöse Behandlung durchgeführt werden.
Ab einem Risiko von über 10 % soll eine nicht nur den Knochenabbau hemmende sondern eine den Knochenaufbau steigernde Behandlung durchgeführt werden.
Für den Score verwenden wir eine freizugängliche App (BVOU Osteoporoserechner). Sie können Ihr Osteoporoserisiko also auch selbst abschätzen. Teilweise wird aber für die Angaben ein medizinisches Fachwissen erwartet. Die Schweregrade vorangegangener Wirbelbrüche werden z.B. nach Genant eingeteilt. Am einfachsten ist es, Sie füllen den über die Anmeldung oder die Internetseite verfügbaren Fragebogen aus und meine Mitarbeiterinnen errechnen Ihr Osteoporoserisiko.
Alarkawi, Dunia, u.a. „Impact of osteoporotic fracture type and subsequent fracture on mortality: the Tromsø Study.” Osteoporosis International 31.1 (2020): 119-130.
Bliuc, Dana, u.a. „Risk of subsequent fractures and mortality in elderly women and men with fragility fractures with and without osteoporotic bone density: the Dubbo Osteoporosis Epidemiology Study.” Journal of bone and mineral research 30.4 (2015): 637-646.
Cotts, Kamala Gullapalli, und Adam S. Cifu. „Treatment of osteoporosis.” Jama 319.10 (2018): 1040-1041.
Hammoudi, L., u. a. „Effects of 2 years endurance training targeted at the level of maximal lipid oxidation on body composition.” Science & Sports (2020).
Heuchemer, L., u.a. „Schmerztherapie bei Osteoporose.” Der Orthopäde (2020): 1-14.
Genant, Harry K., u.a. „Vertebral fracture assessment using a semiquantitative technique.“ Journal of bone and mineral research 8.9 (1993): 1137-1148.
https://register.awmf.org/assets/guidelines/183_Osteologie/183-001anw_S3_Prophylaxe-Diagnostik-Therapie-der-Osteoporose_2024-06.pdf
